Connexion client
Connexion
S'inscrire
Créer un compte a de nombreux avantages :
- Voir la commande et suivre l'expédition
- Suivre l'historique des commandes
- Commander plus rapidement
Mon panier
Sous-total du panier
Aucun article dans votre panier.
Langues
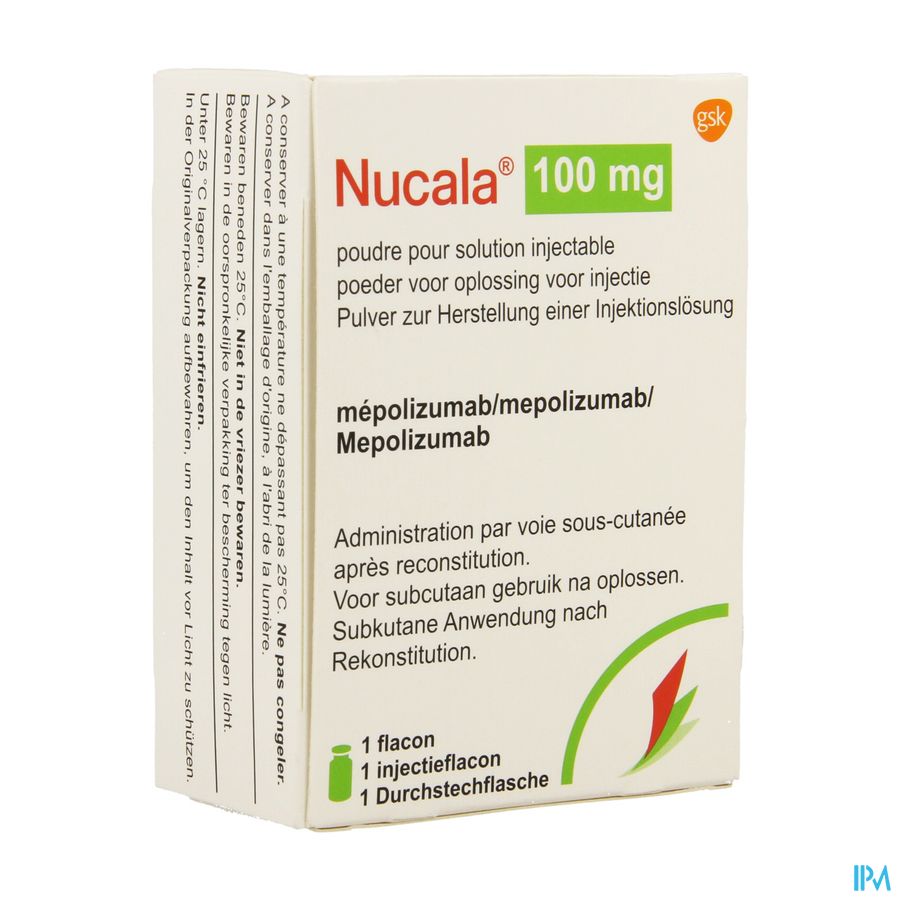
Nucala Pdr Pour Sol Pour Sol Inj Fl 1 X 100mg
éligibles au remboursement
Si vous avez droit au remboursement de ce médicament, vous paierez le taux de remboursement en pharmacie et non le prix affiché sur notre webshop.
Taux de remboursement
€ 12,80 (6% TVA incluse)
Augmentation de la rémunération
€ 8,50 (6% TVA incluse)
Ce produit doit être approuvé par le pharmacien.
Informations importantes
Ce médicament nécessite une ordonnance valide. Il ne peut pas être acheté en ligne et doit être payé à la pharmacie après examen par le pharmacien.
Quantité maximale dans le panier atteinte
Sur demande
4.4 Mises en garde spéciales et précautions d'emploi Traçabilité Afin d'améliorer la traçabilité des médicaments d'origine biologique, le nom et le numéro de lot du produit administré doivent être clairement consignés. Exacerbations d'asthme ou de bronchopneumopathie chronique obstructive Le mépolizumab ne doit pas être utilisé pour traiter les exacerbations aiguës d'asthme ou de BPCO. Des symptômes liés à l'asthme ou à la BPCO,ainsi que des exacerbations peuvent survenir pendant le traitement. Les patients doivent prendre un avis médical si leur asthme ou BPCO reste non contrôlé ou s'aggrave après l'instauration du traitement. Corticoïdes Il est déconseillé d'arrêter brutalement les corticoïdes après l'instauration du traitement par mépolizumab. Si une réduction des doses de corticoïdes est envisagée, celle-ci doit être progressive et réalisée sous le contrôle d'un médecin. Réactions d'hypersensibilité et réactions liées à l'administration Des réactions systémiques immédiates et retardées, incluant des réactions d'hypersensibilité (telles que : anaphylaxie, urticaire, angioœdème, éruption cutanée, bronchospasme, hypotension), ont été observées à la suite de l'administration de mépolizumab. Ces réactions apparaissent généralement dans les heures qui suivent l'administration, mais elles peuvent également survenir plus tardivement (en général après quelques jours). Ces réactions peuvent apparaître pour la première fois alors que le traitement a été initié depuis longtemps (voir rubrique 4.8). En cas de réaction d'hypersensibilité, un traitement approprié adapté au contexte clinique doit être initié. Parasitoses Les éosinophiles peuvent être impliqués dans la réponse immunitaire à certaines helminthoses. Les patients présentant une infestation à helminthes doivent être traités avant l'initiation du traitement. En cas d'infestation parasitaire au cours du traitement par mépolizumab et d'échec au traitement antiparasitaire administré, un arrêt temporaire du traitement doit être envisagé. Patients présentant une BPCO avec un faible taux d'éosinophiles sanguins Les données disponibles ne montrent pas de bénéfice à l'utilisation de Nucala chez les patients présentant une BPCO avec un taux d'éosinophiles sanguins <150 cellules/µL et sans aucune preuve d'une éosinophilie ≥300 cellules/µL au cours des 12 mois précédents. Granulomatose éosinophilique avec polyangéite menaçant un organe ou le pronostic vital Nucala n'a pas été étudié chez les patients avec des manifestations de granulomatose éosinophilique avec polyangéite menaçant un organe ou le pronostic vital (voir rubrique 4.2). Syndrome hyperéosinophilique menaçant le pronostic vital Nucala n'a pas été étudié chez les patients avec des manifestations de syndrome hyperéosinophilique menaçant le pronostic vital (voir rubrique 4.2) Excipients Ce médicament contient du polysorbate 80 (voir rubrique 2), qui peut provoquer des réactions allergiques. Ce médicament contient moins de 1 mmol de sodium (23 mg) pour une dose de 100 mg, c'est-à-dire qu'il est essentiellement " sans sodium ".
Asthme
Chez l'adulte, en traitement additionnel, dans l'asthme sévère réfractaire à éosinophiles.
Chaque seringue préremplie de 1 ml contient 100 mg de mépolizumab.
Contient également : saccharose, phosphate de sodium dibasique heptahydraté, acide citrique monohydraté, polysorbate 80, édétate disodique, eau pour préparations injectables.
4.5 Interactions avec d'autres médicaments et autres formes d'interactions Aucune étude d'interaction n'a été réalisée. Les enzymes du cytochrome P450, les pompes d'efflux et la fixation aux protéines ne sont pas impliqués dans l'élimination du mépolizumab. Une augmentation des concentrations en cytokines pro-inflammatoires (par exemple IL-6) a montré une action inhibitrice sur la formation des enzymes du CYP450 et des transporteurs de médicaments, liée à une interaction avec leurs récepteurs apparentés au niveau des hépatocytes. Néanmoins, l'augmentation des marqueurs pro-inflammatoires systémiques dans l'asthme sévère réfractaire à éosinophiles est faible et aucune expression des récepteurs alpha IL-5 n'a été mise en évidence au niveau des hépatocytes. Par conséquent, le risque d'interactions avec le mépolizumab est considéré comme peu probable.
Comme tous les médicaments, ce médicament peut provoquer des effets indésirables, mais ils ne surviennent pas systématiquement chez tout le monde. Les effets indésirables provoqués par Nucala sont généralement légers à modérés, mais peuvent occasionnellement être graves.
Réactions allergiques Certaines personnes peuvent avoir des réactions allergiques ou de type allergique. Ces réactions peuvent être fréquentes (elles peuvent affecter jusqu'à 1 personne sur 10). Elles surviennent généralement dans les minutes ou les heures suivant l'injection, mais parfois, les symptômes peuvent n'apparaître que plusieurs jours après l'injection.
Les symptômes peuvent inclure : • oppression thoracique, toux, difficulté à respirer, • évanouissements, vertiges, étourdissements (dus à une chute de la pression artérielle), • gonflement au niveau des paupières, du visage, des lèvres, de la langue ou de la bouche, • urticaire, • éruption cutanée.
Consultez immédiatement un médecin si vous (ou l'enfant recevant ce traitement) suspectez une réaction de ce type.
Si vous (ou l'enfant recevant ce traitement) pensez avoir déjà eu une réaction de ce type à la suite d'une injection ou de la prise d'un médicament,
Informez-en votre médecin avant que Nucala ne vous soit administré.
Les autres effets indésirables incluent :
Très fréquents : peuvent affecter plus d'1 personne sur 10 :
• maux de tête
Fréquents : peuvent affecter jusqu'à 1 personne sur 10 :
• infection respiratoire dont les symptômes peuvent inclure toux et fièvre, • infection urinaire (présence de sang dans les urines, mictions douloureuses et fréquentes, fièvre,
douleur dans le bas du dos), • douleur abdominale haute (mal à l'estomac ou sensation de gêne au niveau de la partie
supérieure de l'estomac), • fièvre, • eczéma (plaques rouges sur la peau accompagnées de démangeaisons), • réaction au site d'injection (douleur, rougeur, gonflement, démangeaisons et sensation de
brûlure de la peau à proximité de l'endroit où l'injection a été réalisée), • douleurs au niveau du dos, • arthralgies (douleurs articulaires), • pharyngite (mal de gorge), • congestion nasale (sensation de nez bouché).
Peu fréquents : peuvent affecter jusqu'à 1 personne sur 100 : • zona.
Rares : peuvent affecter jusqu'à 1 personne sur 1 000 :
• réactions allergiques sévères (anaphylaxie).
Contactez immédiatement votre médecin ou votre infirmier/ère si vous constatez l'un de ces symptômes.
4.3 Contre-indications Hypersensibilité à la substance active ou à l'un des excipients mentionnés à la rubrique 6.1.
Grossesse Les données sur l'utilisation du mépolizumab chez la femme enceinte sont limitées (moins de 300 grossesses). Le mépolizumab traverse la barrière placentaire chez les singes. Les études menées chez l'animal n'ont pas mis en évidence de toxicité sur la reproduction (voir rubrique 5.3). Le risque potentiel pour le fœtus humain n'est pas connu. Par mesure de précaution, il est préférable d'éviter l'utilisation de Nucala au cours de la grossesse. L'administration de Nucala chez la femme enceinte ne doit être envisagée que si le bénéfice attendu pour la mère est supérieur au risque éventuel pour le fœtus. Allaitement Il n'existe pas de donnée sur l'excrétion du mépolizumab dans le lait maternel. Toutefois, le mépolizumab a été retrouvé dans le lait de singes femelles Cynomolgus à des taux inférieurs à 0,5 % des concentrations plasmatiques. La décision doit être prise, soit d'interrompre l'allaitement, soit d'interrompre le traitement par Nucala, en tenant compte du bénéfice de l'allaitement pour l'enfant et du bénéfice du traitement pour la femme qui allaite. Fertilité Il n'existe pas de donnée concernant la fertilité chez les humains. Les études effectuées chez l'animal n'ont pas mis en évidence d'effet indésirable d'un traitement anti-IL-5 sur la fertilité (voir rubrique 5.3).
Adultes
- 100 mg, 1 fois toutes les 4 semaines.
- Réévaluation du traitement: au min. 1 fois/an.
- Le patient ne peut pas arrêter brutalement les corticoïdes après avoir débuté le traitement par mépolizumab.
Mode d'administration
- Injection sous-cutanée.
- L'injection peut se faire, soit dans la partie supérieure du bras, soit au niveau de la cuisse ou de l'abdomen.
- Reconstituer avant administration.
-
- Avec 1,2 ml d'eau stérile pour préparations injectables.
- En utilisant de préférence une seringue graduée de 2 à 3 ml et une aiguille de calibre 21G.
- Ne pas secouer la solution pendant la reconstitution (risque de formation de mousse ou de précipitation du produit).
- La solution reconstituée doit être utilisée immédiatement. Si ce n'est pas le cas, elle doit être:
-
- Conservée à l'abri de la lumière.
- Conservée à une température ne dépassant pas 30°C, ne pas congeler.
- Eliminée si elle n'est pas utilisée dans les 8 heures qui suivent la reconstitution.
| CNK | 3434750 |
|---|---|
| Fabricants | SA Glaxosmithkline Pharmaceuticals (GSK) |
| Marques | Gsk |
| Largeur | 73 mm |
| Longueur | 100 mm |
| Profondeur | 43 mm |
| Quantité du paquet | 1 |
| Ingrédients actifs | mépolizumab |
| Préservation | Température ambiante (15°C - 25°C) |